Intégration d'ingrédients dérivés de microalgues dans la formulation de biomatériaux en régénération osseuse
Publié par Nantes Université, le 7 novembre 2024 2.3k
Article écrit par Arnaud Dulom, doctorant au laboratoire RMeS (Médecine Régénératrice et Squelette)
Les défauts du tissu osseux sont très fréquents, peuvent toucher toute la population et sont d’origine variable : infections, tumeurs, chirurgies, génétiques, pathologies et traumatismes. Ainsi, les greffes de tissus osseux sont désormais courantes pour réparer l’os à la suite d’une fracture ou d’autres lésions. Toutefois, cette stratégie présente plusieurs limites, notamment sur la disponibilité du tissu et les risques de réjection et de transmission de maladies lorsque le tissu osseux provient d’un donneur ou d’une autre espèce. Pour ces raisons, depuis de nombreuses années, la communauté scientifique travaille sur le développement de substituts osseux complexes synthétiques ou naturels qui miment le plus fidèlement possible le tissu osseux.
Contrairement aux idées reçues, l’os est un tissu dynamique qui subit un remaniement continue influencé par des sollicitations biologiques et mécaniques ; ce processus s’appelle le remodelage osseux. Ce mécanisme est rendu possible par la coordination de deux fonctions biologiques opposées mais complémentaires : la résorption et la formation osseuse assurées respectivement par les ostéoclastes et les ostéoblastes, deux types de cellules spécifiques du tissu osseux.
Grâce à ce processus l’os présente de véritables propriétés d’autoréparation le rendant capable de se régénérer en cas de lésion. Dans le cas d’une fracture, le réalignement et la stabilisation du site traumatique suffisent généralement à la cicatrisation. Les facultés « ostéogéniques » des ostéoblastes, c’est-à-dire la capacité à produire de l’os par ces cellules, permettent de créer une nouvelle matrice osseuse qui comble le déficit osseux lié à la fracture, restaurant ainsi la fonctionnalité de l’os.
Toutefois, dans certains cas graves de traumatisme (10 % des fractures) le processus de cicatrisation osseuse est insuffisant pour stabiliser et souder la fracture. Par ailleurs, certaines pathologies (comme la pseudo-arthrose ou les maladies parodontales) ou interventions chirurgicales (retrait de tumeurs, kystes, infections) peuvent aboutir à une perte osseuse importante appelée défaut osseux de taille critique que l’organisme seul n'est pas capable de réparer. Dans ces indications de défauts osseux, la reconstruction osseuse doit être médicalement assistée.
Comment réparer ces défauts osseux de taille critique ?
La greffe osseuse est la stratégie de premier choix pour réparer l’os. Dans ce cas, une fraction osseuse peut être prélevée chez le patient, généralement sur la partie supérieure de l’os de la hanche, appelée crète iliaque, puis réimplanter au niveau du trauma pour combler le défaut, on parle d’autogreffe. La sélection de tissu chez le patient lui-même permet de reproduire parfaitement la matrice osseuse, de s’affranchir de réaction immunitaire et de faciliter l’implantation du greffon. Toutefois, la faible disponibilité de tissu osseux pouvant être prélevé comme comblement représente une limite majeure. Ainsi, le greffon osseux peut provenir d’un donneur, on parle alors d’allogreffe. Pour prévenir, des réactions immunitaires le tissu osseux prélevé subi divers traitements pour éliminer les cellules responsables des réactions immunitaires qui résident dans le tissu. Dans ce cas, le tissu implanté n’est pas fonctionnel et sert uniquement de guide à la reconstruction osseuse qui reste malgré tout très limitée.
Ainsi, la recherche travaille depuis de nombreuses années dans le développement de nouveaux substituts osseux présentant des propriétés biologiques et mécaniques similaires à celles du tissu osseux. L’os est un tissu très structuré avec une composante cellulaire qui réside dans une matrice complexe, majoritairement inorganique (cristaux de minéraux, d’hydroxyapatite) associée à une matrice organique avec du collagène minéralisé mais aussi des protéoglycanes couplés à des polymères de sucres (polysaccharides), les glycosaminoglycanes (GAG). Ces polymères ont une importance cruciale dans l’os grâce à leur interaction avec des molécules appelées facteurs de croissance qui stimulent l’ostéogénèse, le processus naturel de formation de l’os. Des études exploratoires dont ce projet de thèse s’intéressent à identifier de nouvelles molécules innovantes analogues de ces GAG pouvant remplir les mêmes fonctions biologiques dans la formulation de substituts osseux.
Exploiter la biodiversité marine dans la santé humaine !
L’utilisation des microalgues en santé est une piste prometteuse, durable et innovante. Les cellules eucaryotes de microalgues peuvent être cultivées dans des photo-bioréacteurs à grande échelle. Leur taux de croissance est rapide et leurs besoins nutritifs proviennent de ressources économiques et renouvelables (eau de mer, CO2 et lumière). En outre, leur production est industrialisable, durable et éthique par l’absence d’exploitation animale. La recherche en bioprocédé développe de nouveaux appareils et infrastructures pour cultiver ces microalgues dans des conditions stériles pour garantir un environnement contrôlé et sécurisé pour des applications futures en santé humaine.
Puis, selon la souche, les microalgues sont capables de produire un large éventail de molécules dont certaines présentent des similitudes avec celles produites chez l’homme. C’est notamment le cas de biopolymères (BioP) proches des GAG naturellement produits par l’Homme dans de nombreux tissus, dont l’os. Ainsi, cette thèse dit de « ressourcement » va s’intéresser à évaluer le potentiel applicatif de ces biopolymères produis par des microalgues dans la régénération osseuse. Les recherches menées en laboratoire ont pour objectif d’identifier l’influence des BioP dérivés de microalgues dans la régénération osseuse par l’évaluation de leur impact sur la production de matrice osseuse, et par la compréhension des mécanismes biologiques régulés. L’objectif final est d’inclure ces molécules marines dans la formulation de biomatériaux dans des applications cliniques pour favoriser la reconstruction osseuse.
Méthodes utilisées pour évaluer l’influence des biopolymères dans la régénération osseuse.
Tout d’abord, il faut vérifier si les BioP de microalgues tout comme les GAG dans la physiologie de l’os, sont capables d’interagir avec des facteurs de croissance impliqués dans la régénération osseuse. Ainsi, des analyses d’interaction moléculaire sont réalisées pour mettre en évidence l’affinité et la force d’interaction entre les biopolymères de microalgues et un des facteurs de croissance principal de la réparation de l’os, utilisé en clinique (OgGF). Dans un second temps, il est important d’évaluer et comprendre quel est l’impact de cette interaction sur le devenir des cellules impliquées dans la cicatrisation osseuse, les ostéoblastes. Pour ces travaux, des Cellules Souches issues de moelle osseuse humaine (hBM-MSCs) sont sélectionnées pour leur capacité à se différencier en ostéoblastes sous l’influence de certains facteurs et produire ainsi de la matrice osseuse. Les cellules hBM-MSCs sont alors traitées dans un milieu ostéogénique associé au cocktail BioP / OgGF et l’efficacité de différenciation sous l’influence de cette association est évaluée par la minéralisation induite par les ostéoblastes. Pour comprendre comment est régulé ce phénomène de différenciation cellulaire des analyses sont menées pour évaluer l’influence de l’interaction sur la bioactivité du facteur de croissance. Une augmentation de la bioactivité et du temps d’action de OgGF en association avec les BioP module l’activation de la voie de signalisation cellulaire responsable de la différenciation ostéoblastique.
Formulation d’un biomatériau utilisant les BioP dérivés de microalgues
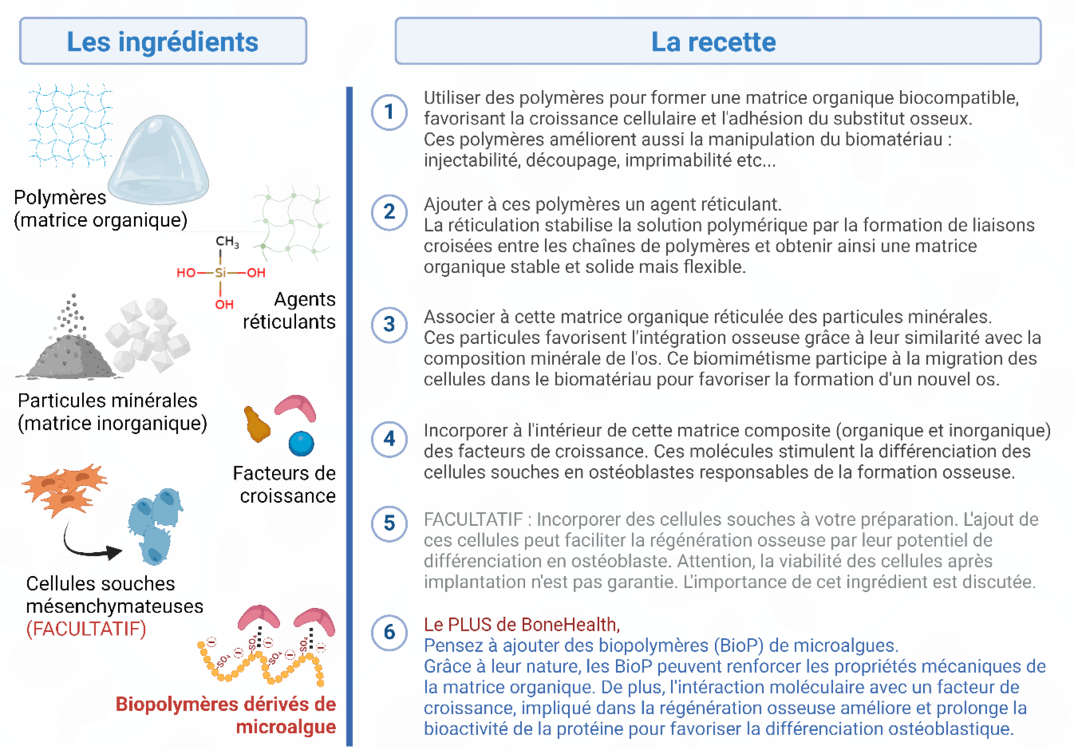
Les biomatériaux servent de support physique aux propriétés mécaniques et biologiques proches du tissu lésé sur lesquels les cellules vont pouvoir adhérer, migrer, proliférer et se différencier pour permettre la repousse osseuse. Ce projet de thèse a comme autre objectif de développer un substitut osseux innovant associé aux BioP de microalgues les plus prometteurs. Des travaux sont réalisés pour trouver la meilleure formulation d’un biomatériau hybride avec une partie inorganique associée à une matrice organique composée en partie par les BioP de microalgues. L’apport des BioP dans cette formulation permettrait de développer un substitut osseux, appelé système de délivrance de médicament aux propriétés mécaniques et structurelles proches de l’os capable de libérer progressivement OgGF au niveau du site traumatique. L’existence d’un tel système repose sur l’interaction spécifique caractérisé entre les BioP et OgGF. L’intérêt d’un relargage progressif de OgGF est d’induire sur du long terme la différenciation ostéoblastique pour stimuler la réparation osseuse au niveau d’un défaut osseux de taille critique.
En conclusion, cette thèse est un projet collaboratif et interdisciplinaire entre différents laboratoires académiques et industriels qui valorise l’utilisation d’ingrédients dérivés de microalgues issus d’une production durable en santé dans le contexte de la réparation osseuse.